На выставке «Химия» представили эффективные решения и проекты «под ключ»
Зюзькова Юлия Геннадьевна , научный сотрудник лаборатории физиологии, молекулярной и клинической фармакологии Научно-исследовательского института фармакологии и регенеративной медицины имени Е. Юлия Геннадьевна в г. С г. Зюзькова Ю.









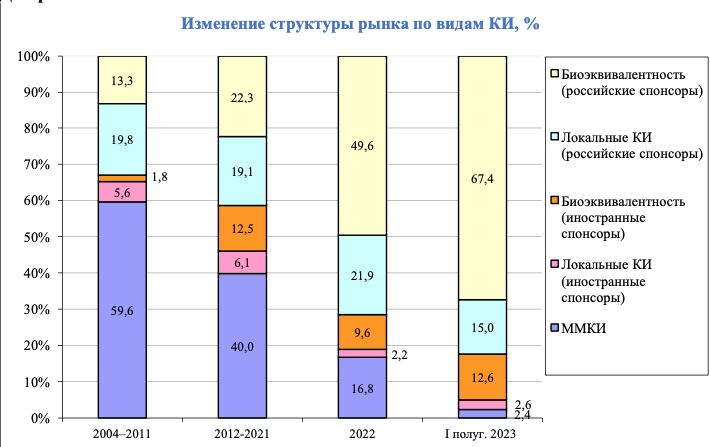
Рынок международных клинических исследований резко сократился в году. В мае на такие исследования выдано шесть разрешений, а средний показатель за предыдущие годы был 19, с 1 по 22 июня года было всего три одобрения, средний показатель за июнь — Об этом на встрече с логистами, организованной компанией Corex, рассказала директор Ассоциации организации по клиническим исследованиям АОКИ Светлана Завидова.




Маркса,3, г. Курск kurskmed mail. Одной из основных задач, возложенных на Комитеты по этике разного уровня, является защита прав, достоинства, интересов и здоровья участников клинических исследований лекарственных средств. Региональный этический комитет далее РЭК создан и функционирует при ФГБОУ ВО КГМУ Минздрава России и призван обеспечить соблюдение этических норм и интересов участников исследований лекарственных средств, проводимых на базе медицинских организаций, научно-исследовательских и образовательных медицинских учреждений Курской, Орловской, Белгородской областей. РЭК включает две секции: клинических и доклинических исследований. В своей деятельности РЭК руководствуется основными принципами проведения клинических и доклинических исследований и действующими международными и российскими нормативными актами:.






